
 |
|||
ųŪ─▄┴„¾w╠Ä└Ē«aŲĘĦ─·ū▀Ą├Ė³▀hĖ³┐ņ
Smart fluid handling to take you forward,faster |
|||
|
╣ż╦ćĘ┼┤¾Ż║┤ŅĮ©šµš²Ą─ĘŌķ]ŽĄĮyęįīŹ¼FCGT«aŲĘęÄ─Ż╗»╔·«a
║┴¤oę╔å¢Ż¼╔·╬’ųŲ╦ÄĄ─Ž┬ę╗éĆ¤ß³cüĒūįį┘╔·ßtīWĪŻÅ─ARM 2020Ą─ę╗Ę▌ĮyėŗöĄō■üĒ┐┤Ż¼╚ź─Ļ╚½Ū“ėą│¼▀^1,085╝ęÅ─╩┬į┘╔·ßtīWĄ─╣½╦ŠŻ¼Ųõųą├└ć°ęį543╝ę╬╗Šė╚½Ū“╩ū╬╗ĪŻųąć°ę▓ęįĮ³300╝ę╬╗┴ąĄ┌Č■Ż¼│¼▀^┴╦ÜWų▐ĪŻ Ę┼č█╚½Ū“Ą─╝Ü░¹┼c╗∙ę“ų╬»¤Ż©CGTŻ®ŅIė“Ż¼├┐─Ļ┤¾Ė┼ėą1,000éĆ┼R┤▓īŹ“×į┌▀MąąŻ¼═¼ĢrFDA├┐─ĻĢ■╩šĄĮ│¼▀^200éĆIND╔ĻšłĪŻĖ∙ō■Accentureī”CGT╩ął÷Ą─ŅA£yŻ¼ĄĮ2030─ĻŻ¼½@┼·╔Ž╩ąĄ─CGT«aŲĘöĄ┴┐īóĢ■▀_ĄĮ60éĆŻ¼▒╚2025─ĻĄ─ŅA£yĘŁ┴╦3▒ČĪŻ ▀@Š═ĦüĒę╗éĆå¢Ņ}Ż║╬ęéā╚ń║╬─▄ėąą¦Ūęų„äėĄžį┌Č╠Ģrķgā╚īó»¤Ę©░▓╚½┐ņ╦┘ĄžÄ¦Įo╗╝š▀Ż┐ ī”ė┌ųąąĪą═CGT╣½╦ŠüĒšfŻ¼Ė▀╦┘į÷ķLĄ─╠¶æį┌ė┌─┐Ū░Ą─ęÄ─Ż¤oĘ©ØMūŃ╔·«aĪŻöĄō■ŅA£y┐╔─▄Ģ■ėą│¼▀^65%Ą─╣½╦ŠĢ■┐╝æ]▐DŽ“Ą┌╚²ĘĮ╝╝ągĘ■äš╣½╦Š═Ō░³ĪŻąĶŪ¾Ą─»B╝ėīó░čē║┴”▐DęŲĄĮ─Ūą®įŁ▒ŠąĪęÄ─ŻĄ─CDMO/CRO╣½╦ŠĪŻ ▀@ą®ę“╦žČ╝┐╔─▄Ģ■ų▒Įėī¦ų┬«aŲʤoĘ©╚ńŲ┌═Č╚ļ╩ął÷ĪŻėąą®«aŲĘĄ─čą░lėŗäØ┐╔─▄Ģ■▒╗═Ų▀tŻ¼ĮKī¦ų┬▓Ī╗╝¤oĘ©Ą├ĄĮßtų╬ĪŻį┌▀@┤╬Ą─ą┬╣┌ę▀ŪķųąŻ¼Å─śIš▀Š═ī”▀@éĆ├¼Č▄╔Ņėą¾wĢ■ĪŻ ╬ęšJ×ķŻ¼ĮŌøQęÄ─Żå¢Ņ}Ą─ĘĮĘ©į┌ė┌╣ż╦ćĄ─ā×╗»║═Ę┼┤¾ĪŻ
╠ß╔²╣ż╦ćĘ┼┤¾Ą─ą¦┬╩
╬ęéā┐╔ęį═©▀^ę╗éĆ│ŻęŖĄ─└²ūėüĒ└ĒĮŌ╣ż╦ćĘ┼┤¾Ż║į┌ę╗ķ_╩╝Ż¼čąŠ┐╚╦åT╩╣ė├å╬═©Ą└ęŲę║śīŻ¼╚╗║¾į÷╝ė│╔8═©Ą└ęŲę║śīŻ¼║¾öU┤¾ĄĮ12═©Ą└Ą─ļŖūėęŲę║śīĪŻ ▀@éĆ▀^│╠╩Ūķ_Ę┼Ą─Ż¼Č°Ūęęį╚╦åT▓┘ū„×ķų„Ż¼ąĶę¬═©▀^ŁhŠ│┐žųŲüĒ┤_▒Ż¤oŠ·Śl╝■ĪŻ«ö▀M╚ļąĪįćļAČ╬Ż¼╬ęéāķ_╩╝ė├┐╔ęįĘ┼┤¾Ą─ĘŌķ]ŽĄĮyüĒ┤·╠µ96┐ū░ÕŻ¼▒╚╚ńąĪą═Ą─╝Ü░¹╣żÅS╗“Ę┤æ¬Ų„ĪŻį┌╝Ü░¹┼ÓBĄ─▀^│╠ųąŻ¼▀ĆąĶę¬Ņ~═Ō┐žųŲpH║═╚▄觥╚ĻPµIę“╦žĪŻ ▀@Š═╩Ū╣ż╦ćĘ┼┤¾Ą─▀^│╠Ī¬Ī¬Å─īŹ“×╩ę╝ēäeĄĮĘ┤æ¬Ų„Ż¼╚╗║¾į┘ę╗▓Į▓Įį÷╝ėĘ┤æ¬Ų„Ą─¾wĘeĪŻ └²ūėųąķ_Ę┼ŽĄĮyĄ─┴ėä▌į┌ė┌Ż¼├┐ę╗éĆ▓Į¾EČ╝ąĶę¬ę└┘ć▓┘ū„╚╦åTĄ─Įø“ׯ¼š¹éĆ▀^│╠Ą─▓╗┐╔┐žąį▌^Ė▀Ż¼ī”▓┘ū„╚╦åTĄ─ę¬Ū¾ę▓Ė³Ė▀Ż¼├┐┤╬Ą─ĮY╣¹Č╝ėą┐╔─▄╩▄ĄĮ╚╦×ķė░ĒæĪŻ ▀@ą®╠¶æ┤¾┤¾ūĶĄK┴╦╣ż╦ćĘ┼┤¾Ą─ą¦┬╩ĪŻ╠žäe╩Ūį┌ųąįć║═╔·«aļAČ╬Ż¼ķ_Ę┼ŽĄĮyĄ─┴ėä▌Š═Ė³╝ė├„’@ĪŻ

«ö╚╗Ż¼¤oŠ·▓┘ū„ę▓╩Ūę╗éĆå¢Ņ}ĪŻąĪęÄ─ŻĄ─ŽĄĮy┐╔ęį═©▀^īė┴„šų╗“│¼ā¶┼_üĒīŹ¼FŠų▓┐¤oŠ·ŁhŠ│ĪŻĄ½ļSų°ę╗┤╬ąį╝╝ągĄ─░lš╣Ż¼ę╗ą®ųŲ╦Ä╣½╦Šų▓Įķ_╩╝īóĻPµI▓Į¾Eė├ĘŌķ]ŽĄĮy┤·╠µŻ¼Å─ķ_Ę┼ŽĄĮy▐Dūā×ķ░ļĘŌķ]ŽĄĮyĪŻ
░ļĘŌķ]ŽĄĮyļm╚╗į┌ę╗Č©│╠Č╚╔Žā×╗»┴╦╣ż╦ć┴„│╠Ż¼Ą½ėąą®ąĶꬤoŠ·▓┘ū„Ą─▓┐Ęų╚į╚╗ę└┘ćīė┴„šųų«ŅÉĄ─įOéõüĒ┐žųŲŁhŠ│ĪŻ░ļĘŌķ]ŽĄĮyę▓¤oĘ©═©▀^ūįäė╗»┐žųŲŽĄĮyī”š¹éĆ╣ż╦ćģóöĄ▀Mąąėøõø║═┐žųŲĪŻ
╬ęéā┐éĮY┴╦CGTŲ¾śIį┌╣ż╦ćĘ┼┤¾Ą─▀^│╠ųą┐╔─▄Ģ■ė÷ĄĮĄ─ÄūéĆ╠¶æŻ║ 1,╚▒╔┘ŽÓī”ę╗ų┬Ą─╣ż╦ć┴„│╠Ż¼Ę┼┤¾ŠĆąįŽĄöĄ▓ŅŻ¼Ė³ČÓĄ─╩Ūę└┘ć╚╦╣ż▓┘ū„ĪŻ▀@ę▓ī”╚š║¾š¹éĆ╔·«a╔Žūį┐žŽĄĮyĦüĒ┴╦ūĶĄKĪŻ 2,Ų¾śIī”ė┌Ģrķg╣سcĄ─░č╬š╚▒Ę”Įø“ׯ¼Ą½╩Ūėų│ą╩▄ų°│╔▒Šęį╝░«aŲĘ╔Ž╩ąĄ─ē║┴”ĪŻė╔ė┌CGT╩Ūę╗éĆą┬┼dĄ─ŅIė“Ż¼║▄ČÓĢr║“Ų¾śIį┌├■ų°╩»Ņ^▀^║ėŻ¼ī”ė┌╣ż╦ćĄ─═Ų▀Mę▓Ģ■▒╚▌^▒Ż╩žŻ¼Ū░Ų┌▓╗╠½įĖęŌ╗©╠½ČÓĄ─═Č┘Yį┌╣ż╦ćā×╗»║═╔²╝ē╔ŽĪŻ 3,╚▒╔┘╩ņŠÜĄ─▓┘ū„╚╦åTĪŻ▓╗āH╩ŪCGTŻ¼š¹éĆ╔·╬’ųŲ╦ÄąąśIę“×ķ╩ął÷į÷ķL╠½┐ņŻ¼Č╝╚▒╔┘īŻśI╚╦åTĪŻį┌┬Ü╚╦åT▒žĒÜ│¼žō║╔╣żū„Ż¼ķLŲ┌ęį═∙Ģ■ė░Ēæ╣żū„ą¦┬╩ĪŻ▀@éĆ╚╦▓┼╚▒┐┌▀ĆīóļSų°Ž┬ę╗éĆ¤ß³cĄ─üĒ┼R│ų└m╝ė┤¾ĪŻ 4,«öūį╔Ē«a─▄▓╗ūŃĢrŻ¼╬ęéāĢ■ŽļĄĮšęCDMO/CRO║Žū„Ż¼Ą½╩Ū▀@▒Š╔Ēę▓╩Ūę╗éĆ╠¶æĪŻšęšl║Žū„Ė³║Ž▀mŻ┐CDMO─┐Ū░ūį╔ĒĄ─«a─▄ę▓į┌ĮėĮ³’¢║═Ż¼╚ń╣¹öU«aätąĶꬹ┬Į©ÅSĘ┐Ż¼▀@īó╗©┘MĖ³ČÓĄ─Ģrķg║══Č┘Y│╔▒ŠĪŻ
ĘŌķ]ŽĄĮyŻ║╣ż╦ćĘ┼┤¾Ą─╝čĘĮ░Ė
╔Ž╩÷Ą─▀@ą®╠¶æ┐╔ęį═©▀^ĘŌķ]ŽĄĮyüĒæ¬ī”ĪŻ Ą┌ę╗Ż¼╗∙ė┌ę╗┤╬ąį╝╝ągŻ©SUTŻ®Ą─ĘŌķ]ŽĄĮy┐╔ęįīŹ¼F¬Ü┴óĄ─ĪóŅÉ╦ŲØŹā¶╩ęĄ─▒ŻšŽĪŻ ▒Ŗ╦∙ų▄ų¬Ż¼Ė─įņę╗éĆØŹā¶╩ęĄ─│╔▒ŠĘŪ│ŻĖ▀░║Ż¼ė╚Ųõ╩ŪA╝ēØŹā¶╩ęĪŻ▀@ę▓╩Ū×ķ╩▓├┤║▄ČÓŲ¾śIĢ■┐╝æ]═©▀^īė┴„šųüĒīŹ¼FŠų▓┐¤oŠ·ŁhŠ│ĪŻĄ½╩Ū╚ń╣¹╩╣ė├ĘŌķ]ŽĄĮyŻ¼ČÓėÓĄ─╗©┘MŠ═▓╗┤µį┌┴╦ĪŻ╗∙ė┌SUTĄ─ĘŌķ]ŽĄĮyī”▓┘ū„ŁhŠ│ø]ėą╚╬║╬ę¬Ū¾Ż¼──┼┬į┌GMP C╝ēŁhŠ│Ž┬ę▓┐╔ęįīŹ¼F¤oŠ·▓┘ū„ĪŻė╔ė┌╩Ūę╗┤╬ąį╩╣ė├Ż¼ŽĄĮy¤oąĶŪÕŽ┤“×ūCŻ¼ø]ėąĮ╗▓µ╬█╚ŠŻ¼ĮĄĄ═’LļUĪŻ╔·«a╣ż╦ćųąĄ─▓┘ū„╚╦åTĄ─░▓╚½ę▓─▄▒╗Ė³║├Ąž▒ŻūoŻ¼╩╣╣żū„ł÷ĄžĖ³Ę¹║ŽEHSę¬Ū¾ĪŻ
īŹ¼Fšµš²Ą─ĘŌķ]ŽĄĮy ╬ęšJ×ķŻ¼«ö╦∙ėąĄ─║─▓─Š∙×ķŅAĮMčbŻ¼▓┼─▄īŹ¼Fšµš²Ą─ĘŌķ]ŽĄĮyĪŻ
ęįā╔ĘN│ŻęŖĄ─╣żą“▀BĮėĘĮ╩Įū„×ķ▒╚▌^Ż║
¤ß╦▄╣▄+║Ė╣▄ÖCŻ║
- ąĶę¬ūįąą▓┘ū„║ĖĮė▀^│╠ĪŻ - ║ĖĮėĢr║“ąĶę¬ė├ĄČŲ¼ŪąĖŅŻ¼Ė▀£žĢ■ī¦ų┬▄ø╣▄öÓ┴čŻ¼┐╔─▄Ģ■░l╔·╚▄│÷╬’║═Ņw┴Ż╬’╬█╚ŠĪŻ - ¤ß╦▄╣▄āHŽ▐ė┌╣▄ÅĮę╗ų┬Ą─═¼╣▄▓─Ż¼╔§ų┴Ž▐ė┌═¼ŲĘ┼Ų═¼ą═╠¢ų«ķg▓┼─▄ē“¤ß║Ė▀BĮėĪŻ - ąĶę¬Ņ~═ŌĄ─║Ė╣▄ÖCįOéõĪŻ
¤oŠ·▀BĮėŲ„Ż║
- ▀BĮė▓Į¾E║å╗»ų┴╔┘3▓ĮŠ═─▄═Ļ│╔Ż¼▀^│╠āHąĶÄū├ļŻ¼▓┘ū„’LļUśOĄ═ĪŻ
- ┐╔ęįį┌į┌ĘŪ¤oŠ·ŁhŠ│Ž┬īŹ¼F¤oŠ·ī”ĮėĪŻ - ▀BĮė▓┐╬╗╩Ū¤oŠ·ĮėŅ^Č°ĘŪ╣▄┬ĘŻ¼ę“┤╦ī”╣▄▓─╣▄ÅĮŠ∙ø]ėąę¬Ū¾Ż¼┐╔ęįį┌╚╬ęŌĄ─╣▄▓─ķg▀BĮė┼cūāÅĮĪŻ - į┌│Ż£žŁhŠ│Ž┬▓┘ū„Ż¼▓╗ė░Ēæ╣▄┬Ę▒Š╔ĒĪŻ - ▓╗ąĶę¬Ņ~═ŌĄ─įOéõ╝ė╣╠ĪŻ ė╔┤╦┐╔ęŖŻ¼¤oŠ·▀BĮėŲ„ū„×ķę╗ĘNSUTŻ¼┐╔ęįį┌ŽĄĮyĻPµIĄ─▀BĮė╠Ä┤¾Ę∙£p╔┘▓┘ū„’LļUĪó║å╗»▓┘ū„┴„│╠Ż¼▒▄├ŌŽĄĮy▒®┬Č▓ó╩▄ĄĮ╬█╚ŠŪų║”Ż¼šµš²ū÷ĄĮ╚½Ī░ĘŌķ]Ī▒ĪŻ

╔Žė╬╝Ü░¹┼ÓB 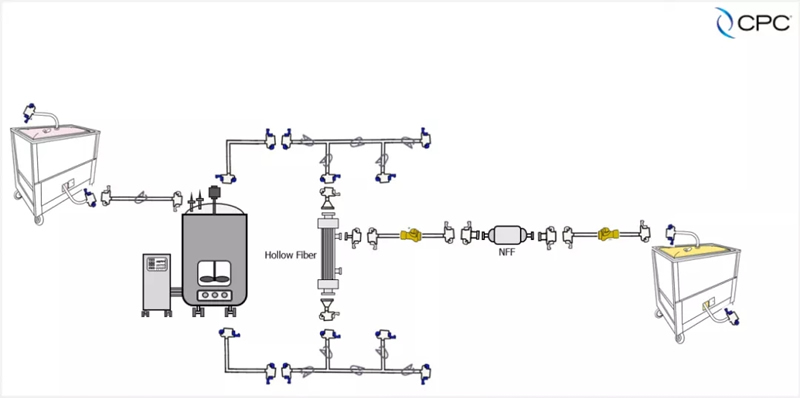
Ž┬ė╬╝ā╗»▀^×V
¤oŠ·▀BĮėĄ─Ųõ╦³ų„ę¬ā×ä▌░³└©Ż║ - ▀BĮėŲ„Įø▀^═Ļš¹“×ūCŻ¼ā╚╚▌░³└©┐╔╠ß╚Ī╬’“×ūCĪó¤oŠ·“×ūCĪóĄ═£žā÷┤µ“×ūCĪóē║┴”£yįćĪó▒¼ŲŲ£yįćĪó╚õūā£yįćĪóžō▌d£yįćĄ╚Ż¼ėąų·ė┌ĮĄĄ═╔·╬’Ų¾śIĄ─“×ūC│╔▒ŠĪŻ - Å─ėąąįäeĄĮ¤oąįäeĄ─▓╗Ęų╣½─Ė¤oŠ·▀BĮėŲ„Ż¼┐╔ęįšf╩Ūę╗éĆ└’│╠▒«╩ĮĄ─ūāĖ’ĪŻī”▓╔┘ÅüĒšfŻ¼╬’┴Ž╣▄└Ē│╔▒ŠĮĄĄ═ę╗░ļŻ╗ī”▓┘ū„╚╦åTüĒšfŻ¼¤oąįäeį┌╩╣ė├Ģr│÷Õe┬╩ę▓Ė³Ą═ĪŻ
CGT╣ż╦ćųąąĶę¬╩╣ė├ĄĮSUTĄ─ŪķŠ░ėą║▄ČÓĪŻ▒╚╚ńūį¾w╣żą“║═▓ĪČŠ▌d¾wĄ─╔·«aŻ¼├┐ę╗▓Į▀BĮėČ╝ąĶę¬║Ž▀mĄ─╝╝ągęį┤_▒ŻŲõ░▓╚½║═Ė▀ą¦ĪŻėų▒╚╚ńį┌▓ĪČŠ▌d¾w╔·«a▀^│╠ųąŻ¼Å─▌d¾wĘ┼┤¾║═ĘNūė┼Óė²ĄĮ╔·╬’Ę┤æ¬Ų„ųąĄ─▌d¾wöUį÷Ż¼į┘ĄĮ│╬ŪÕ║═╝ā╗»Ż¼║¾▀Mąą▀^×V║═╣ÓčbŻ¼īóŲõĄ╣╚ļ│╔ŲĘ╚▌Ų„ųąŻ¼├┐ę╗▓Į▓┘ū„Č╝ąĶę¬▀BĮė╝╝ągĄ─ų¦│ųĪŻ
╝┤╩╣į┌ę╗ĘN▓┐╝■ŅÉą═ųąŻ©╚ńā”ę║┤³ĪóĮėŅ^╗“╝Ü░¹┼ÓBŽĄĮyŻ®ųąŻ¼SUT Ą─öĄ┴┐Č╝╩Ū¾@╚╦Ą─ĪŻę“┤╦Ż¼ą┬ė├æ¶Ģ■ĮøÜvę╗éĆČĖŪ═Ą─īW┴ĢŪ·ŠĆĪŻ╬ęéā╣─äŅCGTŲ¾śIŽ“īŻśIĄ─┴„¾w╠Ä└ĒīŻ╝ęįö╝Ü┴╦ĮŌ▀m║Ž─·æ¬ė├Ą─ SUTų¬ūRĪŻ
 ģó┐╝┘Y┴Ž [1] ARM 2020 State of the Industry Report [2] Srivastava S. How Cell And Gene Therapy Is Transforming Healthcare, Cell & Gene, Feb. 2020
CPC│╔┴óė┌1978─ĻŻ¼╩Ū╔·╬’ųŲ╦ÄĪó╝Ü░¹║═╗∙ę“ų╬»¤╩ął÷Ą─ę╗┤╬ąį▀BĮėŲ„╝╝ągĄ─ŅIŽ╚įOėŗ║═ųŲįņ╔╠ĪŻCPCīŻūóė┌čą░lßśī”╔·╬’║═į┘╔·ßtīW╩ął÷Ą─ĮėŅ^«aŲĘŻ¼į┌╔·╬’ųŲ╦ÄŅIė“ėą│¼▀^20─ĻĄ─Įø“×ĪŻ┐╝æ]ĄĮąąśIĄ─’w╦┘░lš╣║═┐═æ¶▓╗öÓį÷ķLĄ─ąĶŪ¾Ż¼CPCĮ±─Ļ└^└möU╚▌é}ÄņŻ¼į÷╝ė░▓╚½Äņ┤µĪŻ
|
||||||||||||||||||
We inspire confidence at every point of connection.
Š®╣½ŠW░▓éõ11010502019739 |
ĻāICPéõ11000581╠¢-1
| ┬ōŽĄ╬ęéā |
|
 ╝ė╬ę╬óą┼ |
 ╣½▒Ŗ╠¢ |
|||||||||||||||
|
||||||||||||||||||